Kalorymetria, dziedzina fizyki zajmująca się pomiarami ciepła, odgrywa kluczową rolę w wielu aspektach naszego życia, od codziennego ogrzewania budynków po zaawansowane zastosowania inżynieryjne i naukowe. Zrozumienie zasad wymiany ciepła i ciepła właściwego pozwala na projektowanie efektywnych systemów grzewczych, analizę procesów termicznych w reaktorach, a nawet na tworzenie innowacyjnych materiałów. Niniejszy artykuł zgłębia praktyczne zastosowania kalorymetrii, przedstawiając liczne przykłady i zadania, które ilustrują jej znaczenie.
Skale Temperatury i Ich Ewolucja
Historia pomiaru temperatury sięga początków XVIII wieku. W roku 1701 duński astronom Ole Rømer zaproponował skalę temperatury opartą na dwóch stałych punktach. W jego skali woda zamarzała w 7,5 stopniach, a wrzała w 60 stopniach. Choć ta konkretna skala nie przyjęła się powszechnie, stanowiła ważny krok w kierunku standaryzacji pomiarów temperatury, poprzedzając bardziej znane skale, takie jak Celsjusza czy Fahrenheita.

Termiczna Ekspansja Materiałów w Inżynierii
Różnice w rozszerzalności cieplnej materiałów stanowią istotne wyzwanie w projektowaniu inżynieryjnym. Inżynierowie muszą brać pod uwagę, jak zmiany temperatury wpływają na wymiary i naprężenia w konstrukcjach.
Jednym z takich problemów jest zaprojektowanie struktury, w której różnica w długości pomiędzy belką stalową a belką aluminiową pozostaje zawsze równa 0,5 m, niezależnie od zmian temperatury w zwykłym zakresie. Jest to zadanie wymagające precyzyjnego doboru materiałów i geometrii.
Inny przykład dotyczy naprężeń powstających w belce stalowej, gdy jej temperatura zmienia się od -15°C do 40°C, a belka jest unieruchomiona i nie może się rozszerzać. W takiej sytuacji pojawiają się naprężenia ściskające. Dla stali o module Younga E = 210⋅10⁹ N/m², naprężenie można obliczyć, uwzględniając współczynnik rozszerzalności cieplnej stali.
Mosiężny pręt o średnicy 0,8 cm i długości 1,2 m, zamocowany na dwóch końcach, również podlega naprężeniom w wyniku zmian temperatury. Przy module Younga E = 90⋅10⁹ N/m² i temperaturze początkowej 25°C, wzrost temperatury spowoduje naprężenia rozciągające, a spadek temperatury naprężenia ściskające.
Kalorymetria w Życiu Codziennym i Eksperymentach
Zasady kalorymetrii znajdują zastosowanie w codziennych sytuacjach, a także w prowadzonych eksperymentach naukowych.
Przykład z życia: Wyobraźmy sobie sytuację, w której ciastko zostało pozostawione w lodówce, a następnie chcemy je ogrzać do temperatury pokojowej. Jeśli zamiast tego konsola do gry, która pracowała przez dłuższy czas, jest gorąca, a ciastko zimne, możemy zastosować zasady kalorymetrii do analizy wymiany ciepła. Wkładając gorącą konsolę do torby z ciastkiem i talerzykiem, tworzymy swego rodzaju kalorymetr. Po osiągnięciu równowagi termicznej w temperaturze 38,3°C, możemy wyliczyć ilości przekazanego ciepła. Mając masę konsoli (2,1 kg) i jej temperaturę początkową (45°C), masę ciastka (0,16 kg) i jego ciepło właściwe (3 kJ/kg°C), masę talerzyka (0,24 kg) i jego ciepło właściwe (0,9 kJ/kg°C), oraz temperaturę początkową ciastka i talerzyka (4°C), możemy analizować bilans cieplny.
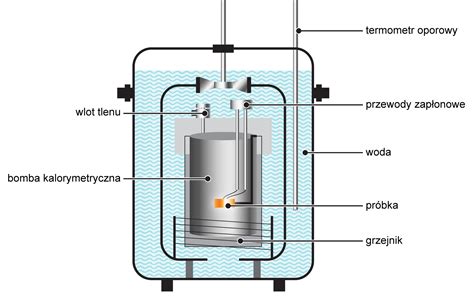
Eksperymentalne wyznaczanie ciepła właściwego: Określenie ciepła właściwego substancji, na przykład wody, nie musi być trudne i wymagać specjalistycznej aparatury. Można to przeprowadzić, mierząc, jak szybko źródło ciepła o znanej mocy jest w stanie podgrzać określoną ilość wody i o jaką temperaturę. Ilość dostarczonej energii możemy zmierzyć za pomocą źródła ciepła o znanej mocy P i poprzez pomiar czasu jego pracy τ. Czajnik lub grzałka elektryczna, gdzie cała energia elektryczna zamieniana jest na ciepło, są idealnymi narzędziami do tego celu.
Masę wody można wyznaczyć za pomocą wagi lub mierząc jej objętość, korzystając ze znajomości gęstości wody. Temperaturę początkową mierzymy termometrem, a temperaturę końcową przyjmujemy jako moment rozpoczęcia wrzenia (100°C), głównie ze względów bezpieczeństwa.
Ilość ciepła wytworzonego przez grzałkę obliczamy ze wzoru: Q₁ = W = P ⋅ τ.Ciepło pobierane przez wodę powoduje wzrost jej temperatury zgodnie ze wzorem: Q₂ = m ⋅ cw ⋅ Δt = m ⋅ cw ⋅ (100°C - tpoczątkowa).Zakładając brak strat energii, równanie bilansu ciepła przyjmuje postać: Q₁ = Q₂ , co prowadzi do: P ⋅ τ = m ⋅ cw ⋅ (100°C - tpoczątkowa).Z tego równania można obliczyć ciepło właściwe wody: cw = (P ⋅ τ) / (m ⋅ (100°C - t_początkowa)).
Doświadczenie 1 - Wyznaczenie ciepła właściwego wody: W praktycznym doświadczeniu, moc grzałki (P) i czas jej pracy (τ) są odczytywane z tablic znamionowych i mierzone stoperem. Masę wody można zmierzyć wagą lub menzurką. Zmierzona temperatura początkowa wody (t_początkowa) i moment rozpoczęcia wrzenia pozwalają na obliczenie ciepła właściwego. Należy pamiętać o potencjalnych źródłach błędów, takich jak straty energii do otoczenia, niedokładność przyrządów pomiarowych czy błędy w odczycie czasu. Zbyt późne wyłączenie stopera powoduje zawyżenie obliczonej wartości ciepła właściwego, gdyż ciepło dostarczone po rozpoczęciu wrzenia nie powoduje dalszego wzrostu temperatury wody, a jedynie jej parowanie.
Polecenie 3: Grzałka o mocy 1,5 kW (1500 W) ogrzewa 1,5 litra (1,5 kg) wody o temperaturze początkowej 20°C przez 3 minuty (180 s). Przyjmując ciepło właściwe wody cw = 4200 J/(kg·°C) i pomijając straty energii, temperaturę końcową można obliczyć.Q = P ⋅ τ = 1500 W ⋅ 180 s = 270 000 J.Q = m ⋅ cw ⋅ Δt270 000 J = 1,5 kg ⋅ 4200 J/(kg·°C) ⋅ ΔtΔt = 270 000 / (1,5 ⋅ 4200) ≈ 42,86 °C.Temperatura końcowa = 20°C + 42,86°C = 62,86°C.
Polecenie 4: W naczyniu znajduje się 1 litr (1 kg) wody o temperaturze 80°C. Chcemy uzyskać temperaturę końcową 50°C, dodając wodę o temperaturze 10°C.Niech m₂ będzie masą dodanej wody.Bilans cieplny: m₁ ⋅ cw ⋅ (T₁ - Tk) = m₂ ⋅ cw ⋅ (Tk - T₂).1 kg ⋅ (80°C - 50°C) = m₂ ⋅ (50°C - 10°C).1 ⋅ 30 = m₂ ⋅ 40.m₂ = 30 / 40 = 0,75 kg.Należy wlać 0,75 kg wody o temperaturze 10°C. Aby dokładnie obliczyć masę potrzebnej wody, należałoby uwzględnić straty energii do otoczenia oraz ewentualne zmiany objętości wody wraz ze zmianą temperatury.
Polecenie 5: Do 1 litra (1 kg) wody o temperaturze 20°C wrzucono bryłkę szkła o masie 0,19 kg, która była wcześniej w naczyniu z wrzącą wodą (100°C). Po chwili temperatura wody wzrosła do 23,1°C. Ciepło właściwe wody cw = 4200 J/(kg·K).Ciepło oddane przez bryłkę = Ciepło pobrane przez wodę.mszkło ⋅ cszkło ⋅ (Tbryłka - Tk) = mwoda ⋅ cw ⋅ (Tk - Twoda).0,19 kg ⋅ cszkło ⋅ (100°C - 23,1°C) = 1 kg ⋅ 4200 J/(kg·K) ⋅ (23,1°C - 20°C).0,19 ⋅ cszkło ⋅ 76,9 = 1 ⋅ 4200 ⋅ 3,1.14,611 ⋅ cszkło = 13020.c_szkło = 13020 / 14,611 ≈ 891 J/(kg·K).
Przewodnictwo Ciepła i Izolacja Termiczna
Zrozumienie przewodnictwa cieplnego jest kluczowe dla efektywnego ogrzewania i izolacji budynków.
Okna z podwójnymi szybami: Obliczanie szybkości przewodzenia ciepła przez okno z podwójnymi szybami wymaga uwzględnienia oporu cieplnego poszczególnych warstw. Dla okna o powierzchni 1,5 m², z szybami o grubości 0,8 cm i przerwą powietrzną 1 cm, przy temperaturze wewnętrznej 15°C i zewnętrznej -10°C, należy najpierw obliczyć spadek temperatury na każdej z szyb, a następnie na przerwie powietrznej. Przewodnictwo cieplne powietrza jest znacznie niższe niż szkła, co czyni podwójne szyby lepszym izolatorem.
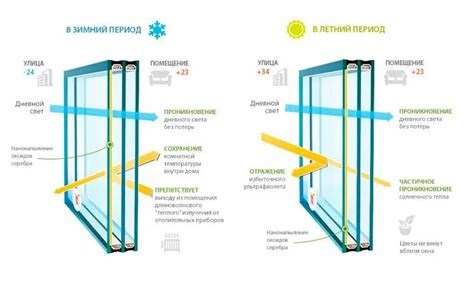
Obliczenie szybkości przewodzenia ciepła przez pojedyncze okno o grubości szkła 1,6 cm, o tej samej powierzchni i w tych samych temperaturach, pozwoli na porównanie efektywności izolacyjnej.
Ściana zewnętrzna domu: Zewnętrzna ściana domu o wysokości 3 m i szerokości 10 m, składająca się z płyty kartonowo-gipsowej (R=0,56), warstwy włókna szklanego (10 cm) i izolacji (R=2,6), stanowi złożony system izolacyjny. W bardziej realistycznym scenariuszu, uwzględniającym drewniane belki (4 cm grubości, 10 cm szerokości, rozmieszczone co 40 cm), przepływ ciepła będzie zależał od oporu cieplnego poszczególnych materiałów i ich rozmieszczenia.
Przewodnictwo ciepła przez tkankę ludzkiego ciała: Nawet tkanka ludzkiego ciała przewodzi ciepło. Przy grubości 3 cm, różnicy temperatur 2°C i powierzchni skóry 1,5 m², można obliczyć szybkość przewodzenia ciepła.
Kolba Dewara: Kolba Dewara, będąca skutecznym izolatorem, blokuje wymianę ciepła z wyjątkiem górnej powierzchni. W przypadku zamrażania wody w takiej kolbie, tworzy się lód. Woda i dolna powierzchnia lodu mają temperaturę 0°C, podczas gdy górna powierzchnia lodu ma temperaturę powietrza w zamrażarce (-18°C). Szybkość przepływu ciepła przez lód można przyjąć jako równą szybkości straty ciepła podczas zamarzania wody.
Promieniowanie Cieplne
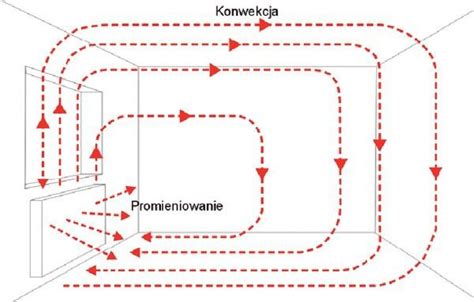
Promieniowanie cieplne jest kolejnym ważnym mechanizmem wymiany ciepła.
Grzejnik podczerwieni: Grzejnik podczerwieni do sauny o powierzchni 0,05 m² i zdolności emisyjnej 0,84, wymagający mocy 360 W, musi działać w określonej temperaturze. Można ją obliczyć, stosując prawo Stefana-Boltzmanna dla promieniowania.
Moc promieniowania Słońca: Natężenie promieniowania docierającego do Ziemi wynosi 1370 W/m². Na podstawie tej wartości można oszacować moc promieniowania emitowanego przez Słońce, uwzględniając odległość między Słońcem a Ziemią.
Zastosowania w Chłodnictwie i Energetyce
Kalorymetria znajduje zastosowanie również w procesach chłodniczych i energetycznych.
Schładzanie mleka ciekłym azotem: W niektórych krajach mleko w cysternach jest schładzane ciekłym azotem. Obliczenie ilości przekazanego ciepła potrzebnego do odparowania LN2 i podniesienia jego temperatury do 3°C wymaga znajomości ciepła parowania i ciepła właściwego azotu.
Reaktor jądrowy: Po wyłączeniu reaktor jądrowy wciąż produkuje energię cieplną o mocy 150 MW. Ta pozostała moc cieplna musi być odprowadzana, aby zapobiec przegrzaniu.
Produkcja amunicji: Pasjonaci strzelania, którzy sami produkują pociski, topiąc ołów i wlewając go do form, wykorzystują procesy związane z ciepłem topnienia i krzepnięcia metali.
Topnienie lodu: Żelazny cylinder o masie 0,8 kg i temperaturze 103°C, umieszczony w izolowanej skrzynce z 1 kg lodu w temperaturze topnienia, spowoduje częściowe lub całkowite stopienie lodu, a następnie podgrzanie powstałej wody. Bilans cieplny pozwoli określić końcową temperaturę układu.
Kostka lodu w kalorymetrze: Kostka lodu o masie 30 g w temperaturze topnienia, wrzucona do aluminiowego kalorymetru (100 g) z 300 g nieznanej cieczy (24°C), prowadzi do końcowej temperatury 4°C. Pozwala to na wyznaczenie ciepła właściwego nieznanej cieczy.
Temperatura topnienia lodu
Kalejdoskop Zastosowań Kalorymetrii
Kalorymetria, poprzez analizę wymiany ciepła i ciepła właściwego, dostarcza fundamentalnej wiedzy niezbędnej do rozwiązywania problemów inżynieryjnych, projektowania efektywnych systemów energetycznych i izolacyjnych, a także do prowadzenia badań naukowych. Od prostych doświadczeń edukacyjnych po zaawansowane zastosowania przemysłowe, zasady kalorymetrii pozostają niezmiennie ważne w naszym dążeniu do zrozumienia i kontrolowania zjawisk termicznych.
Tagi: #kalorymetria #ogrzewanie #zadania